แบบฝึกหัดบทที่3
1. จำนวนพันธะโคเวเลนต์ในโมเลกุล CH4 , SiCl4 , NaCl , NH3 เป็นกี่พันธะมีค่าเรียงตามลำดับ คือข้อใด
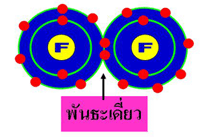
2. พันธะเดี่ยว หมายถึงอะไร
ก. พันธะที่เกิดจากการใช้เวเลนซ์อิเล็กตรอนร่วมกัน 1 คู่
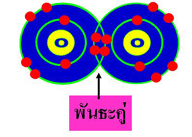
ข. พันธะที่เกิดจากการใช้เวเลนซ์อิเล็กตรอนร่วมกัน 2 คู่
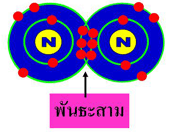
ค. พันธะที่เกิดจากการใช้เวเลนซ์อิเล็กตรอนร่วมกัน 3 คู่
ง. พันธะที่เกิดจากการใช้์อิเล็กตรอนคู่โดดเดี่ยวร่วมกัน 1 คู่
3. ธาตุในข้อใด เกิดพันธะโคเวเลนต์กับธาตุคลอรีนได้ดีที่สุด
ก. Na ข. Ra ค. C ง. Cs
4. สมบัติทางกายภาพในข้อใด ที่ใช้อธิบายสมบัติทางเคมีของอโลหะ
ก. พลังงานไอออไนเซชันสูง ขนาดอะตอมใหญ่ สัมพรรคภาพอิเล็กตรอนน้อย
ข. พลังงานไอออไนเซชันต่ำ ขนาดอะตอมใหญ่ อิเล็กโทรเนกาติวิตีต่ำ
ค. พลังงานไอออไนเซชันสูง ขนาดอะตอมเล็ก สัมพรรคภาพอิเล็กตรอนน้อย
ง. พลังงานไอออไนเซชันสูง ขนาดอะตอมเล็ก อิเล็กโทรเนกาติวิตีสูง
5. ธาตุ Z มีพลังงานไอออไนเซชันตั้งแต่ลำดับที่หนึ่งถึงลำดับที่ 8 เป็นดังนี้ 1.320, 3.395, 5.307, 7.476, 10.996, 13.333, 71.343, 84.086 ธาตุ Z มีเวเลนซ์อิเล็กตรอนเท่าใด
ก. 1 ข. 4 ค. 6 ง. 7
6. ตารางแสดงค่าพลังงานพันธะเฉลี่ยในสารไฮโดรคาร์บอน
ชนิดพันธะ | พลังงานพันธะ |
C - H | 413 |
C - C | 348 |
ก. มากกว่า 587 kJ ข. น้อยกว่า 283 kJ ค. มากกว่า 526 kJ ง. น้อยกว่า 278 kJ
7. เหตุใดสารโคเวเลนต์ จึงมีจุดเดือด จุดหลอมเหลวต่ำ
ก. สารโคเวเลนต์มีแรงยึดเหนี่ยวระหว่างโมเลกุลน้อย ข. สารโคเวเลนต์มักสลายตัวได้ง่าย
ค. สารโคเวเลนต์ไม่มีประจุไฟฟ้า ง. สารโคเวเลนต์มักมีโมเลกุลขนาดเล็ก
8. สารละลายที่เกิดจากธาตุหมู่ 1 กับน้ำ มีสมบัติอย่างไร
ก. เป็นกลาง ข. เป็นได้ทั้งกรดและเบส ค. เป็นกรด ง. เป็นเบส
9. สาร X เป็นโมเลกุลไม่มีขั้ว สาร Y เป็นโมเลกุลมีขั้ว ส่วนสาร Z เป็นพันธะไม่มีขั้ว ถ้าขนาดของโมเลกุลของ X>Y>Z แล้วสาร X Y และ Z ควรเป็นดังข้อใด
ก. CH2 , NH3 , C6H6 ข. BeCl2 , CH2Cl2 , S8 ค. Br2 , H2O , H2 ง. SiH4 , PCl3 , PCl5
10. กำหนดค่า EN ของธาตุดังนี้ A = 3.0 , B = 2.8 X= 2.7 , Y = 3.7 จงเรียงลำดับความแรงขั้วจากมากไปน้อย
ก. A-B , B-X , X-Y ข. A-Y , B-X , A-X ค. Y-B , A-Y , A-X ง. A-X , B-Y , A-Y
11. ถ้า A , B และ C เป็นสารโคเวเลนต์ 3 ชนิด โดยทั้ง 3 ชนิดมีสถานะเป็นของเหลว โมเลกุลของสาร Aและ B มีขั้ว ส่วนโมเลกุลของสาร C ไม่มีขั้ว สารใดสามารถละลายน้ำได้
ก. สาร C ข. สาร A และ C ค. สาร A เเละ B ง. สาร B และ C
12. จงระบุว่าสารในข้อใดละลายน้ำได้
1) แคลเซียมคลอไรด์ 2) แอมโมเนียมซัลเฟต 3 )เมอร์คิวรี(I)คลอไรด์
4) ไอร์ออน(III)ไฮดรอกไซด์ 5) โพแทสเซียมฟอสเฟต
ก. 1 2 3 ข. 1 2 5 ค. 2 3 4 ง. 2 3 5
13. ถ้า A, B ,C ,D เป็นธาตุที่มีเลขอะตอม 7,11,17 และ 20 ตามลำดับ สูตรของไอออนและสารประกอบไอออนิกในข้อใดถูกต้อง
ข้อ | ไอออนบวก | ไอออนลบ | สูตรสารประกอบไอออนิก |
ก | D2+ | A3- | D3A2 |
ข | C3+ | B2- | C2B3 |
ค | B+ | A- | BA |
ง | A+ | C- | AC |
ก. พันธะในสาร X เป็นพันธะไอออนิก
ข. เมื่อ X ละลายน้ำ จะดูดความร้อน ทำให้ละลายได้น้อย
ค. X มีสูตร CaF2 ผลึกมีความแข็งแรงมากจึงละลายได้ยาก
ง. สาร X เมื่อหลอมเหลวจะนำไฟฟ้า
15. เมื่อละลาย KCl ในน้ำเกิดปฏิกิริยาเป็นขั้น ๆ และมีการเปลี่ยนแปลงพลังงาน ดังนี้
1) KCl(s) -----> K+(g) + Cl-(aq) H1 = 701.2 kJ/mol
2) K+(g) + Cl-(g) -------> K+(aq) + Cl-(aq) H2 = 684.1 kJ/mol
ปฏิกิริยานี้เป็นแบบใด
ก. คายพลังงานเท่ากับ 1385.3 kJ/mol ข. คายพลังงานเท่ากับ 17.1 kJ/mol
ค. ดูดพลังงานเท่ากับ 17.1 kJ/mol ง. ดูดพลังงานเท่ากับ 1385.3 kJ/mol
16. สาร X , Y , Z มีพลังงานพันธะเป็น 120 , 200 , 90 kJ/mol ตามลำดับ จงเรียงความยาวพันธะจากน้อยไปมาก
ก. X , Y , Z ข. Z , Y , X ค. Y , X , Z ง. Z , X , Y
17. ข้อใดกล่าว ไม่ ถูกต้องเกี่ยวกับสมบัติของสารประกอบไอออนิก
ก. นำไฟฟ้าได้ทุกสถานะ ข. เกิดจากการรวมตัวของไอออนบวกกับไอออนลบ
ค. จัดเรียงตัวเป็นผลึก ง. มีผลรวมของประจุสุทธิ เป็น ศูนย์
18. พันธะเคมี หมายถึง อะไร
ก. แรงยึดเหนี่ยวระหว่างอะตอม ข. พลังงานที่ทำให้อะตอมสลายตัว
ค. การอยู่รวมกันของอะตอม ง. การอยู่รวมกันของโมเลกุล
19. กำหนดการจัดอิเล็กตรอนของธาตุให้ ดังนี้ A 2,8,2 B 2,8,8,1 C 2,8,7 D 2,8,18, 8 ธาตุคู่ใดมีการเกิดเป็นสารประกอบไอออนิกได้
ก. A กับ D ข. C กับ D ค. B กับ C ง. B กับ D
ก. อโลหะมีค่า EN สูงเสียอิเล็กตรอนยาก ข. อโลหะมีค่า EN สูงเสียอิเล็กตรอนง่าย
ค. อโลหะมีค่า EN ต่ำเสียอิเล็กตรอนยาก ง. อโลหะมีค่า EN ต่ำเสียอิเล็กตรอนง่าย